Att lyssna på hjärnan med bättre precision och mindre skada
För att bättre förstå hur hjärnan fungerar och vad som händer när den drabbas av olika sjukdomar behöver vi kunna lyssna på hjärnan. Vi måste kunna göra det utan att skada den samtidigt som vi har koll på vilka hjärnceller som vi faktiskt lyssnar på. Först då kan vi studera vilka celler som är aktiva vid kronisk smärta eller följa vad som verkligen händer när någon drabbas av exempelvis Alzheimers sjukdom eller depression. Med ökad precision kan vi också stimulera hjärnan på ett mer exakt sätt och med mycket färre biverkningar än idag, exempelvis för att hämma skakningar vid Parkinsons sjukdom. Snart finns hjärnelektroder som faktiskt uppfyller dessa krav.
– Vi behöver utveckla elektroder som gör det möjligt att studera hjärnan, och helst enskilda celler utan att skada dem. Syftet är att lära sig hur hjärnan fungerar och hur saker hänger ihop. Det kommer att öppna för helt nya behandlingsmöjligheter, säger Jens Schouenborg, neurofysiolog och professor vid Neuronano Research Center vid Lunds universitet.
Problemet med de flesta elektroder som används idag är att de är stela, och ofta ganska grova, vilket gör att de irriterar hjärnvävnaden när hjärnan rör sig – vilket den gör mer eller mindre hela tiden, som när vi andas eller rör på huvudet. Elektroden skaver helt enkelt mot den omgivande hjärnvävnaden vilket leder till ärrbildning runt elektroden, en så kallad ”kill-zone” med döda nervceller. Och då har man skadat det man ville studera.
”Elektroderna är så tunna att de inte ens klarar av att bryta ytspänningen på en vattenyta.”
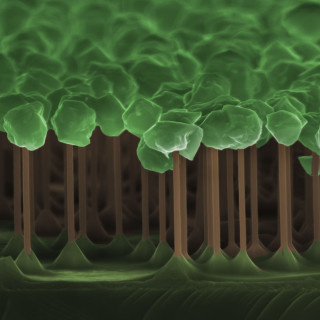
Jens Schouenborg och hans forskargrupp har under en längre tid jobbat med att utveckla tunnare och smidigare elektroder som kan följa med i hjärnans naturliga rörelser. Det visade sig att tunna, flexibla elektroder med ungefär samma densitet som hjärnvävnaden orsakade minst skada. Elektroderna är dock så tunna att de inte ens klarar av att bryta ytspänningen på en vattenyta. För att göra det möjligt att föra in dem i hjärnan bäddas elektroderna in i gelatin. Gelatinet är skonsamt mot hjärnan, ger inte upphov till någon ärrbildning och löser upp sig när elektroden väl är på plats.
Försöken är hittills bara gjorda på råttor men den nya tekniken öppnar för möjligheter att kunna registrera vad som händer i hjärnan hos ett djur som är vaket och rör sig, och kunna göra det under längre tid, upp till flera månader.
– Det här var ett genombrott för flexibla implantat. Vi lyckades visa att det går att föra in supertunna flexibla elektroder i hjärnan utan att skada den, att vi har näst intill obefintliga kill-zones runt implantat av den här typen. Vi har också visat att elektroderna fungerar och att de kan behålla sin struktur. Det sista är en förutsättning för att vi ska kunna registrera signaler från samma celler under en längre tid.

Jens Schouenborg, neurofysiolog och professor vid Neuronano Research Center vid Lunds universitet.
Hittills har forskarna jobbat i mikroskala men nu när det finns en fungerande metod med flexibla elektroder som inte skadar hjärnan börjar det bli intressant att försöka få det att fungera även i nanoskala. Nano, som är en miljondels millimeter, erbjuder möjligheter att studera olika förlopp mera i detalj. Vad gäller nervceller öppnas möjligheter att exempelvis detaljstudera nervcellernas synapser (kontaktytan mellan två nervceller där signalöverföringen sker).
– Just nu håller vi på att nanostrukturera de supertunna, flexibla elektroderna, säger Jens Schouenborg lite kryptiskt.
Mer vill han inte avslöja just nu. Vad han däremot kan berätta är att man i samarbete med fysiker vid Neuronano Research Center lyckats tillverka och implantera en nanoelektrod, en elektrod med supertunna nanotrådar, i hjärnan på en råtta och kunnat fånga upp signaler från nervcellerna. Nöten som återstår att knäcka är att göra de nanotrådsbaserade elektroderna lika flexibla som de i mikroskala.
SUPERTUNNA FLEXIBLA ELEKTRODER som kan placeras exakt där forskarna vill ha dem och som registrerar signaler från enskilda eller några få celler är intressanta verktyg för grundforskningen men vilka medicinska tillämpningar ligger i pipeline?
Det som är kliniskt intressant idag är stimulering av olika områden i hjärnan. Metoden har tillämpats under ganska lång tid på patienter med Parkinsons sjukdom för att dämpa de skakningar som är förenade med sjukdomen. Problemet med dessa elektroder är att de är ganska grova (i millimeterskala) och stela vilket leder till ärrbildning i hjärnan. Det i sin tur medför att större strömstyrka behöver användas för att nå utanför kill-zonen vilket gör elektroderna oprecisa – och då berörs dessutom även andra områden i hjärnan vilket ger biverkningar.
Eftersom de nya flexibla elektroderna inte ger upphov till någon kill-zone kan man jobba med lägre strömstyrka och därmed åstadkomma mer exakt stimulering med färre biverkningar.
– Vår plan är att utveckla elektroder som sätts in och spretas ut i vävnaden. Varje elektrod kommer att stimulera ett litet område. Vi kommer att kunna avläsa vilka av elektroderna som ger önskad effekt och de kommer vi att fortsätta använda medan de som ger biverkningar kommer att stängas av.
Ett annat intressant område är att studera vad som händer i hjärnan vid kronisk smärta för att i förlängningen kunna utveckla skräddarsydda läkemedel.
– Vi vill utveckla en användbar modell för att kunna testa smärtlindring, idag mäter man inte rätt saker, säger Jens Schouenborg.
För att få en korrekt bild bör man mäta hur nervceller i hjärnbarken bearbetar smärtsignaler. Och här kommer de nya, flexibla elektroderna väl till pass.
Text: Eva Bartonek Roxå
Artikeln var först publicerad i Vetenskap & hälsa
Filmen nedan visar hur ett knippe elektroder, som är inbäddade i gelatin, förs in i hjärnan. När elektrodknippet väl är på plats löser gelatinet upp sig och elektroderna spretas ut i vävnaden. Film: Neuronano Research Center.
Filmen nedan visar hur det skulle kunna se ut när nanopartiklar med tillhörande droger frigörs i vävnaden. Film: Neuronano Research Center.